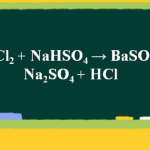BaCl2 là một trong những loại chất được sử dụng rất nhiều trong hóa học. Vậy BaCl2 là chất gì và BaCl2 có kết tủa không? Hãy cùng mình khám phá và tìm hiểu về loại muối này nhé!
Nội dung
BaCl2 là chất gì?
BaCl2 là công thức hóa học của hợp chất vô cơ với tên gọi là Bari Clorua hay Barium Chloride. Đây là một trong những loại muối hòa tan trong nước phổ biến nhất của bari.
Công thức phân tử của Bari Clorua là BaCl2
Công thức cấu tạo BaCl2: Cl-Ba-Cl
Tính chất vật lý của muối BaCl2:
- Đây là chất rắn màu có màu trắng và có khả năng tan tốt trong nước.
- Có độc tính
- Khi đốt cho ngọn lửa có màu xanh lá cây sáng.
Vì thế câu trả lời cho câu hỏi: “BaCl2 có kết tủa không?” là CÓ và nó có màu trắng.
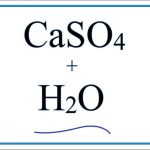
Cách nhận biết muối BaCl2: Khi cho vài giọt H2SO4 vào dung dịch BaCl2 sẽ thấy hiện tượng kết tủa trắng và không tan trong axit.
BaCl2 + H2SO4 → 2HCl + BaSO4
Tính chất hóa học của muối BaCl2
BaCl2 là muối, nên nó mang đầy đủ tính chất hóa học của muối.
Tác dụng với muối
BaCl2 + 2AgNO3 → 2AgCl + Ba(NO3)2
BaCl2 + CuSO4 → BaSO4 + CuCl2
Tác dụng với axit
BaCl2 + Cl2SO4 → BaSO4 + 2HCl
Tính chất khác
- Dễ hòa tan trong nước lạnh cùng methanol, nhưng lại không tan trong ethanol
- Khối lượng mol: 208,23 g/mol ở dạng khan
- Tỷ trọng: 3,856 g/cm3 ở dạng khan
- Độ nóng chảy: 962 oC ở dạng khan
- Điểm sôi: 1560oC
Cách điều chế muối Bari Clorua BaCl2
Thông thường BaCl2 được sản xuất với số lượng lớn dựa trên quá trình trình điều chế từ Bari Cacbonnat hay Hydroxit, sau khi cho phản ứng với axit Clohydric sẽ tạo ra sản phẩm là Bari Clorua ngậm nước.
Trong công nghiệp, muối Bari Clorua BaCl2 sẽ được điều chế từ Bari Sunfat.
BaSO4(s) + 4C(s) → BaS(s) + 4CO(g) (Ở điều kiện nhiệt độ cao)
BaS + CaCl2 → BaCl2 + CaS ( Lưu ý các chất tham gia phản ứng phải ở trạng thái nóng chảy).
Ứng dụng muối BaCl2 trong phòng thí nghiệm và công nghiệp

Do BaCl2 là một loại muối Bari giá rẻ và có thể ta được trong nước, nên Bari Clorua có ứng dụng vô cùng rộng rãi trong phòng thí nghiệm.
Trong phòng thí nghiệm: Được dùng để kiểm tra sự có mặt của các ion sunfat
Trong công nghiệp:
- Được sử dụng chủ yếu trong việc tinh chế dung dịch nước muối trong nhà máy sản xuất clorua caustic và sản xuất muối xử lý nhiệt, thép, hoặc sản xuất bột màu và các loại muối bari khác.
- BaCl2 cũng được dùng trong pháp hoa để tạo màu xanh lá cây sáng, nhưng tính độc của nó đã làm hạn chế khả năng ứng dụng.
- Là nguyên liệu trong sản xuất thuốc diệt chuột và thuốc trừ sâu
- Trong xử lý nước: Có tác dụng loại bỏ CaSO4 ở trong nước nồi hơi
Hướng dẫn cách bảo quản và sử dụng BaCl2 an toàn
Trong quá trình sử dụng và bảo quản BaCl2 người dùng cần lưu ý một số điều sau:
- Bảo quản hóa chất tại nơi thoáng mát, khô ráo và sử dụng các thùng chứa chuyên dụng.
- Tránh bảo quản, xử lý bằng axit hoặc những loại chất oxi hóa khác
- Tuân thủ đầy đủ các quy định về an toàn của hóa chất khi sử dụng.
- Khi bari clorua tan trong nước sẽ vô cùng độc hại, vì vậy các bạn cần lưu ý khi sử dụng. Ngoài ra, bạn có thể sử dụng magie sunfat, natri sunfat để làm thuốc giải độc. Bởi khi tác dụng tạo ra barium sunfat không tan và nó sẽ tương đối không độc hại.
- Trang bị đầy đủ các thiết bị được bảo hộ như kính mắt, gang tay, khẩu trang,… và đặc biệt là không được tiếp xúc trực tiếp với hóa chất.
Trên đây là những thông tin tổng hợp về vấn đề “BaCl2 có kết tủa không” cùng những tính chất và đặc điểm của nó.