Việc trả lời được câu hỏi Na2CO3 có kết tủa không sẽ cung cấp cho bạn những thông tin quan trọng trong quá trình phân tích hóa học. Khi đó, bạn sẽ biết cách sử dụng những phản ứng kết tủa để nhận biết các ion kim loại. Ngoài ra, bạn sẽ ứng dụng nó ra sao trong quá trình sản xuất và công nghiệp. Hãy đọc ngay bài viết dưới đây để nắm tất tần tật các kiến thức trên.
Nội dung
Nguồn gốc của Na2CO3

Tên gọi của Na2CO3 là Natri cacbonat và còn được biết đến với cái tên khác là soda. Đây là loại muối cacbonat của natri, thường xuất hiện nhiều trong tự nhiên như có ở nước biển, nước khoáng và các mỏ muối dưới lòng đất.
Quá trình hình thành Na2CO3 chủ yếu là do sự thay đổi địa hình trái đất khiến cho một số hồ gần biển hoặc vịnh bị thu hẹp lại. Theo thời gian, một lượng lớn muối sẽ bị tích tụ và chôn vùi dưới lòng đất tạo thành các mỏ muối. Phần muối còn lại được tạo ra do sự hòa tan của khí CO2 trong không khí sẽ tồn tại trong tự nhiên (nước biển).
Cấu trúc của Na2CO3
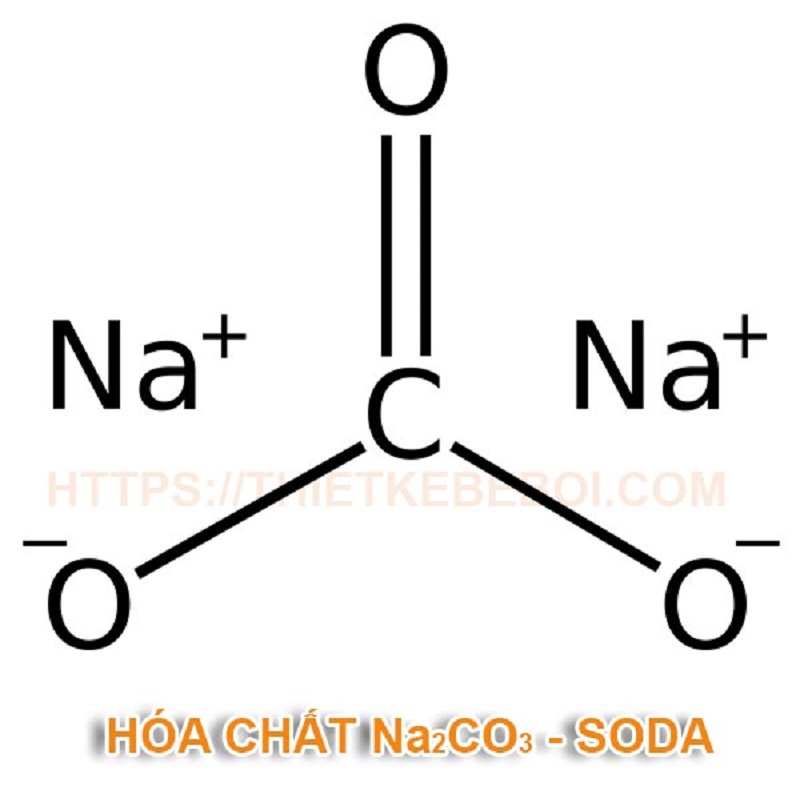
Natri cacbonat (Na2CO3) có khối lượng mol phân tử là 106,0 g/mol. Đây là một muối natri của axit cacbonic được tạo thành từ hai cation natri (Na+) và một anion cacbonat (CO3 2-). Hay nói đơn giản hơn thì Natri cacbonat (Na2CO3) là muối của kim loại Na và có gốc axit yếu CO3.
Na2CO3 có kết tủa không?

Na2CO3 là một muối natri không thể kết tủa, bởi tất cả các muối natri đều hòa tan. Về cơ bản, Na2CO3 khan là chất bột màu trắng, hút ẩm, có mùi nồng. Tuy nhiên, khi Na2CO3 tồn tại lâu trong không khí sẽ bị bốc hơi gây tình trạng chảy nước.
Trong một số phản ứng hóa học, Na2CO3 tạo thành kết tủa muối do gốc CO3 phản ứng với các ion kim loại như Ca2+, Mg2+. Vì vậy, Na2CO3 là hóa chất được sử dụng rộng rãi trong xử lý nước bể bơi, lọc nước hay làm mềm các loại nước.
Ví dụ:
- Cho dung dịch muối Na2CO3 vào ống nghiệm chứa CaCl2. Trong ống nghiệm xuất hiện kết tủa trắng Canxi Cacbonat (CaCO3).
Na2CO3 + CaCl2 → CaCO3 + 2NaCl
- Cho vài giọt dung dịch Na2CO3 vào ống nghiệm chứa 1ml dung dịch Ba(OH)2. Trong ống nghiệm sẽ xuất hiện kết tủa trắng.
Na2CO3 + Ba(OH)2 → 2NaOH + BaCO3
Phản ứng giữa Na2CO3 và một số chất khác có kết tủa không?
BaCl2 + Na2CO3 có kết tủa không?
- Phương trình hóa học: Na2CO3 + BaCl2 → 2NaCl + Ba2CO3
- Kết luận: Xuất hiện kết tủa trắng Ba2CO3
KCl + Na2CO3 có kết tủa không?
- Phương trình hóa học: Na2CO3 + 2KCl → 2NaCl + K2CO3
- Kết luận: Không tạo kết tủa
H2SO4 + Na2CO3 có kết tủa không?
- Phương trình hóa học: Na2CO3 + H2SO4 → Na2SO4 + CO2 + H2O
- Kết luận: Không tạo kết tủa
Na2CO3 có kết tủa màu gì?
Như đã được giải thích ở phía trên, bởi vì Na2CO3 không thể kết tủa được. Chính vì thế, chúng ta sẽ không xác định được màu của Na2CO3 sau khi kết tủa.
Na2CO3 có tan trong nước không?

Na2CO3 là chất dễ tan trong nước, khi hòa tan trong nước sẽ tỏa nhiệt bằng cách tạo thành hydrat. Bên cạnh đó, Na2CO3 là chất ưa nhiệt, nên ở nhiệt độ càng cao thì muối này sẽ càng khô hơn và dần biến thành muối khan.
- Ở nhiệt độ dưới 32,5 độ C, Na2CO3 kết tinh thành Na2CO3.10H2O
- Ở nhiệt độ 32,5 – 37,5 độ C, Na2CO3 kết tinh thành Na2CO3.7H2O
- Ở nhiệt độ trên 37,5 độ C, Na2CO3 kết tinh thành Na2CO3.H2O
- Ở 107 độ C, Na2CO3 mất nước và trở thành muối natri cacbonat khan.
Khi tiếp xúc với không khí, sẽ tạo thành Na2CO3.10H2O (Decahydrat) dễ bị mất nước. Từ đó, hợp chất này sẽ kết tinh và tạo thành Na2CO3.5H2O (một loại bột màu trắng vụn).
Cách điều chế Na2CO3

Đầu tiên, đun nóng hỗn hợp natri sunfat (Na2SO4) với than(C) và đá vôi (CaCO3) ở nhiệt độ cao (khoảng 1000 độ C). Vì vậy có hai phản ứng xảy ra:
- Na2SO4 + 2C → Na2S + 2CO2 (khí)
- Na2S + CaCO3 → Na2CO3 + CaS
Để tách muối natri cacbonat, người ta hòa tan hỗn hợp thu được vào nước để tách CaS không tan.
Tuy nhiên hiện nay, natri cacbonat chủ yếu được điều chế bằng phương pháp amoniac với phương trình hóa học sau:
- NaCl + NH3 + CO2 + H2O → NaHCO3 + NH4Cl
Vì NaHCO3 ít tan trong nước nên nó được tách ra và nhiệt phân tạo thành Na2CO3, CO2.
- 2NaHCO3 → Na2CO3 + CO2 + H2O
Ứng dụng thực tế của Na2CO3

- Tăng độ pH của hồ bơi: Sử dụng lượng Na2CO3 thích hợp vào nước của hồ bơi giúp loại bỏ bụi bẩn và tạp chất có hại. Khi độ PH đạt chuẩn sẽ ngăn chặn tảo, rong rêu phát triển. Nhờ vậy, bể bơi được làm sạch, nước bể bơi sẽ ít bị nhiễm khuẩn hơn.
- Ứng dụng làm chất tẩy rửa: Thường được sử dụng để làm sạch dầu trên các chi tiết máy trong quá trình sơn, phủ kim loại và còn được ứng dụng trong công nghiệp sản xuất chất tẩy rửa.
- Ứng dụng để sản xuất thủy tinh, silicat, xà phòng, công nghiệp bông, sản xuất keo dán gương. Na2Co3 cũng được ứng dụng để làm gạch nhờ cơ chế giảm lượng nước cần thiết để để ép đất sét.
Lưu ý khi sử dụng và bảo quản Na2CO3
- Na2CO3 phải được bảo quản ở nơi khô ráo, thoáng mát
- Không được để gần với axit
- Không nên để trong kho hàng quá lâu vì sẽ ảnh hưởng đến chất lượng sản phẩm
- Khi tiếp xúc với hóa chất, hãy đeo thiết bị bảo hộ cá nhân
Kết luận
Tất cả những thông tin trên đã giải thích chi tiết về hợp chất Na2CO3 và trả lời câu hỏi Na2CO3 có kết tủa không. Cũng như đã giúp các bạn hiểu được các tính năng và ứng dụng của hợp chất này là gì? Hãy ghi chú lại kiến thức hóa học này để áp dụng vào học tập hoặc nơi làm việc của mình ngay.